你知道吗 “水”不是一种液体 而是两种
水(H₂O)
是万物之源
然而我们司空见惯的水
在科学上却是最怪异的液体
甚至于水不是一种液体
而是两种
下面我们来瞧瞧
科学家是如何证实这点的

水具有热缩冷胀的特性,一般情况下,水会在低于0℃的温度下结冰,这都归结于水中通常含有灰尘或其他的可附着的固体类杂质。但是对于纯净的水来说,由于缺乏杂质作为“晶化启动剂”,结冰反而变得更加艰难,它需要一种额外的强有力的推动力,才能迫使分子变成结冰所需的特殊结构。因此水可以在很低的温度下仍然保持液态,这便是所谓的过冷现象。
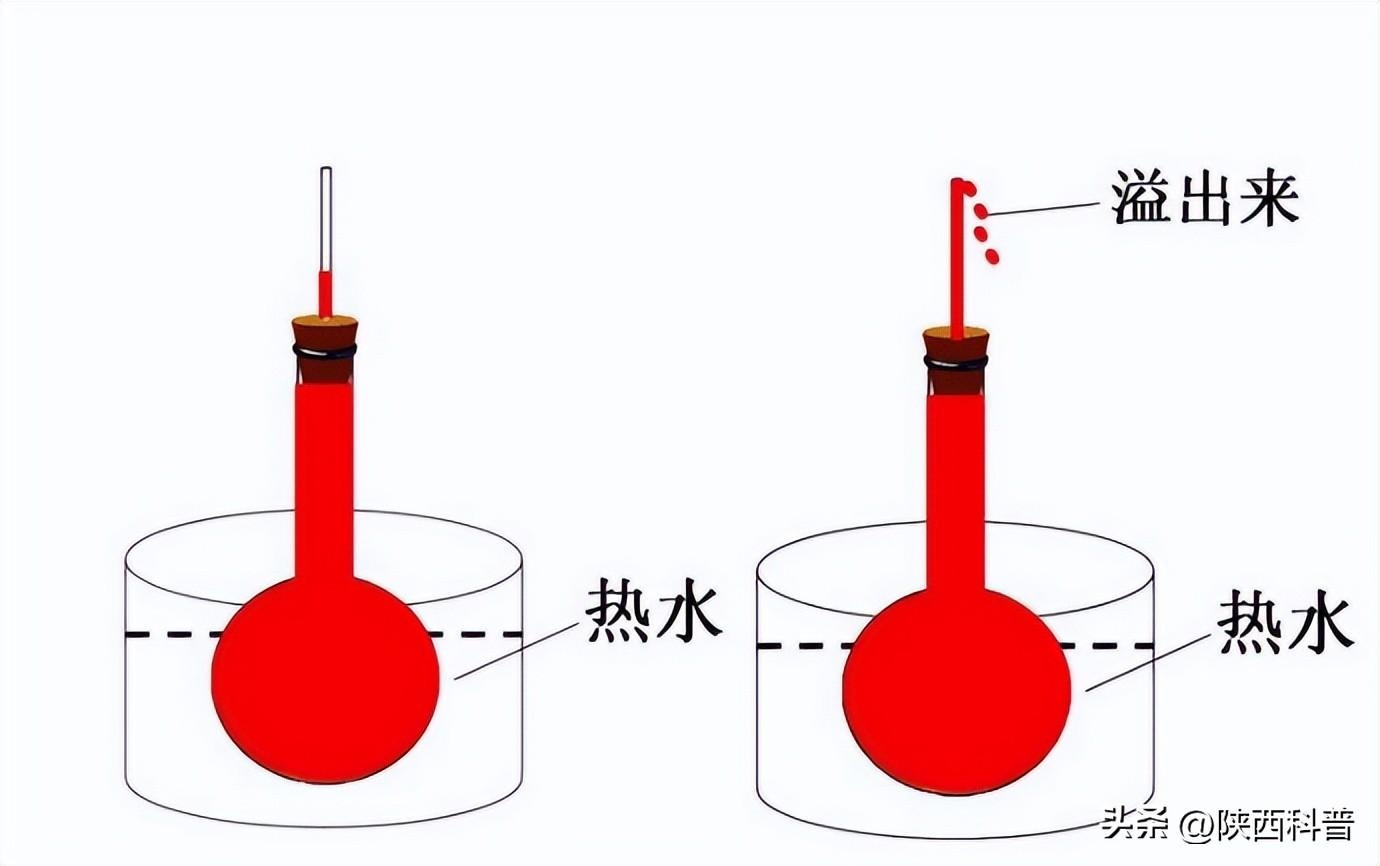
水的热胀冷缩特性
现在,《科学》杂志上刊登了一项新的研究,介绍了一个研究团队在-138℃到-28℃的温度范围内,对液态水进行了一系列测量。他们使用了一种有点像“定格摄影”的实验方法来对过冷液态水拍摄“快照”。实验中,他们用激光对一层水薄膜进行加热,然后迅速让其从-28℃冷却到-83℃,在几纳秒的时间之内就形成过冷的液态水。他们用红外光照射薄膜来观察其中的水分子,分析这些水分子是如何相互推挤的。
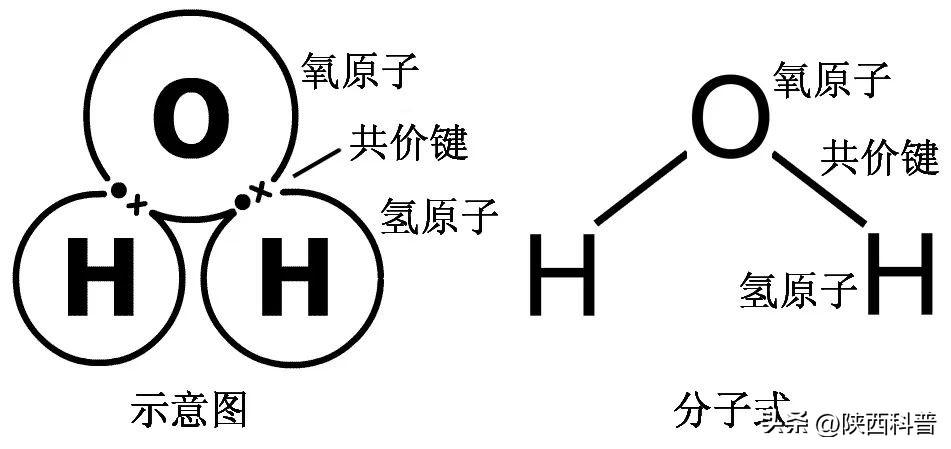
氧原子和氢原子通过共价键结合形成水分子。图源:科普中国
利用这种方法所收集到的数据,他们发现,过冷水在极度低温下不仅相对稳定,而且存在两种结构模体。这表明水分子在氢键的影响下,可以有两种排列方式,按四面体有序排列或随机无序排列,分别组成低密度水和高密度水。
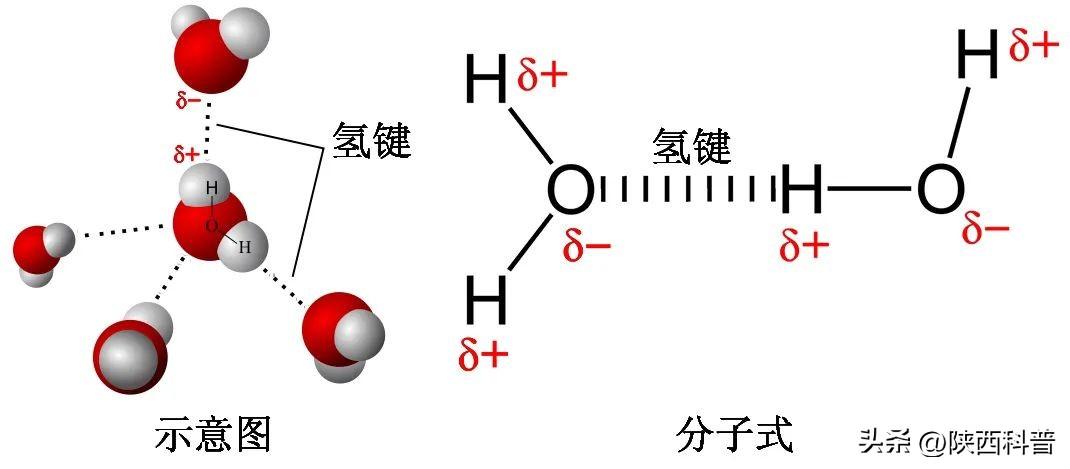
水分子间氢键的形成。图源:科普中国
很神奇吧
除此之外
还有一些关于水的“反常”小知识
冰的密度比水小
冰中的水分子排列方式与低密度水中水分子排列方式相同,即四面体结构,而水中还有无序结构的高密度水,因此,水的平均密度大于冰的密度。

水在4℃时密度最大
在0°C时,水分子更多地处于四面体结构的有序相,即低密度水占优势。极端情况下,如果完全没有无序的高密度水,液态水就结成冰了。温度升高,分子无规则的热运动就越剧烈,有序结构就越少,高密度水越占优势,即水的密度升高。但当温度达到4°C以上时,分子热运动使水分子间距随温度升高而增大,水的密度因而降低。

水的比热容显著大于绝大多数液体
加热物质,使其升高一定量的温度,但水比其他液体需要热量更高,即比热容更大,因为水需要一部分热量来破坏低密度水的四面体结构。
水比绝大多数液体难以被压缩
这是氢键带给水分子之间强烈的吸引力造成的,尤其是对于高密度水。
高压下水分子更易于扩散
高压可破坏四面体有序结构,水分子排列越无序,越易于扩散。

水受热膨胀,加压,更膨胀
加压使水更无序,因而易于膨胀。
当然,水还有更多的反常性质有待揭晓。目前而言,水分子确定有两种排列方式,这个理论与实验相符,且能一致地解释水的反常性质。